引言
肿瘤血管生成是肿瘤进程中普遍的病理现象,直接调控着肿瘤的生长、侵袭、转移等病理过程。肿瘤血管生成,可以为肿瘤细胞带来生长所必须的养分和氧气,并排出代谢废物,同时新生的血管可作为转移的通道介导肿瘤远处转移。实体肿瘤直径超过400微米即需要有新生血管的供给,否则肿瘤会因缺血缺氧而坏死,生长速率明显受限(Folkman,2002)。基于此,抗血管生成己成为肿瘤治疗的重要策略。2009年,一种抗肿瘤血管生成药物-贝伐珠单抗(Bevacizumab)在美国被FDA批准上市,该药物是针对VEGF-A的特异性单克隆抗体,可通过降低血液循环中的VEGF含量而抑制肿瘤血管生成,被用于治疗肺癌、肾癌、卵巢癌等恶性肿瘤(Van der Veldt etal. 2012)。但后续的实验及临床研究都发现,抗血管治疗虽然可以在短时间内起到抑制肿瘤生长、侵袭及转移的作用,但是这种疗效难以保持,并不能明显提高肿瘤患者的总体预后(Vasudevetal.2013)。肿瘤血管生成的具体分子机制至今仍未完全阐明,可能是肿瘤抗血管治疗不能达到理想效果的根本原因之一。血管生成受多种促血管生成因子及抑血管生成因子的调控,在肿瘤生长及转移中发挥着关键作用。目前,有五大蛋白家族被认为是肿瘤血管生成的关键调控因子,即VEGF与其受体家族、血管生成素与Tie受体家族、Notch受体家族、Eph/ephrin家族和Slit酉fi体/Robo受体家族(Ziyad and Iruela-Arispe, 2011)。其中,Ephrin-Al 与其主要受体EphA2作为Eph/ephrin家族的主要成员,不仅在多种恶性肿瘤中明显表达,而且与正常及肿瘤血管生成密切相关。2000年,Ogawa等(2000)第一个报道了EphA2/ephrinAl在肿瘤血管生成中发挥重要作用。我们在对59例行手术治疗的舌癌患者组织标本EphA2表达情况的研究中发现,EphA2与VEGF表达量与微血管密度(MVD)及患者预后高度相关,二者可能在舌癌血管生成中发挥重要作用(Shaoetal. 2008);近期我们对49例人涎腺腺样囊性癌EphA2/ephrin-Al进行了检测,发现其在mRNA及蛋白水平的表达均较正常组织明显上调,且功能高度活跃,与肿瘤MVD、TNM分期、神经侵袭及血管侵袭显著相关(Shao etal. 2013)。肿瘤细胞ephrin-Al的过表达可明显促进肿瘤血管生成过程,而ephrin-Al表达下调则可抑制肿瘤细胞诱导的内皮细胞迁移及降低微血管密度。这在动物实验中也得到了证实,EphA2基因敲除小鼠移植瘤生长体积、诱导血管生成能力及远处转移能力明显降低;将该基因敲除小鼠的内皮细胞进行原代培养,发现该内皮细胞系的迁移及成血管能力降低,说明EphA2在肿瘤血管生成及转移方面发挥重要作用(Brantley-Sieders et al. 2005)。Ephrin-Al促血管生成能力的实现有赖于内皮细胞表面EphA2受体的激活,但是ephrin-Al在肿瘤微环境中究竟是如何被调控的以及其激活EphA2受体后下游信号是如何传导的,目前尚不清楚。
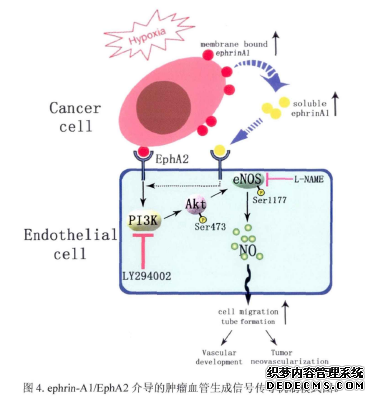
Ephrins的表达受到多种生长因子及细胞因子的调控,如肿瘤坏死因子、白细胞介素等。低氧是肿瘤微环境最重要的特征之一,在肿瘤病理过程中发挥着重要作用,可通过调控多种促血管生成因子的表达影响肿瘤血管生成。低氧诱导因子-1 a(hypoxia-inducible factor,HIF-1 a )是介导肿瘤细胞低氧反应最重要的氧平衡调节因子。有学者证实HIF-la可上调ephrins及Eph在鼠皮肤低氧模型中的表达(Liao andJohnson , 2007)=在头颈癌中也发现,肿瘤组织中ephrin-Al的表达与肿瘤微环境中氧分压的高低密切相关(Liu etal. 2011)。由此可见,Ephrin-Al可能是低氧诱导肿瘤血管生成过程中的关键效应分子,在肿瘤低氧微环境调控血管生成方面发挥着重要作用。但是低氧是否能直接诱导肿瘤细胞产生ephrin-Al而促血管生成仍缺乏直接证据;特别是ephrin-Al已被证实可作为一种可溶性配体从肿瘤细胞表面分泌出来,且仍然保持了激活EphA2受体的生物学活性,探讨低氧对可溶性ephrin-Al表达及活性的影响,可能揭示ephrin-Al通过旁分泌途径激活肿瘤血管生成的新机制。目前,Ephrin诱导血管生成过程中的信号转导机制仍未完全阐明。一些信号分子已经被证实参与了ephrins下游的信号传导,如MAP/ERK、PI3K等。但是MAPK/ERK、PDK/Akt等分子主要是细胞复杂信号转导网络的中介信号分子,可能进一步激活多种目的蛋白,ephrins下游是否有更终末的信号分子或直接效应分子仍知之甚少。一氧化氮(NO)是人体广泛存在的重要信号分子,在血管生成、平滑肌收缩、免疫反应、凋亡及突触传递等方面发挥着重要作用(Hirst and Robson, 2011),而异常的NO活性被认为是心血管疾病病理变化过程中的关键事件。NO可以加速或者抑制肿瘤发生过程,且参与调控肿瘤的血管生成、侵袭及生长。
………
文献综述一 ephr i n-A1 /EphA2在肿瘤中的研究进展
目前的理论认为,肿瘤是含有多种细胞且细胞间相互高度协作的“器官”,其由肿瘤细胞与所谓的间质相互组成,不同细胞通过自身细胞膜表面或胞内质膜上的信号分子感受外界环境的变化,相互间的信号交通形成复杂的信息网络,调控着肿瘤的发生、发展、侵袭、转移等一系列生物学行为(Zlyadand Imela-Arispe,2011)。受体酪氨酸蛋白激酶(receptor tyrosine kinases,RTKs)可以将外界信息传递至细胞核,是细胞将外界刺激转化成生物学行为的信号转导通路中的关键分子,在细胞的分化、增殖、胚胎发育、器官形成和细胞内信号转导过程中起着重要作用。产促红细胞生成素肝细胞瘤受体家族(Erythropoietin-producing hepatoma,Eph)是目前已知最大的受体酷氨酸激酶家族。Eph受体通过与其配体ephrins相互作用,能调节包括组织器官分化成熟、轴突导向、肢芽形成、细胞与细胞间的點附、血管生成及肿瘤发生等生理病理过程(Arvanitis and Davy, 2008)。有研究表明,该家族中的EphA2受体及其配体ephrin-Al在多种恶性肿瘤中表达,且二者的相互作用可明显促进肿瘤血管内皮细胞的迁移,并通过影响细胞骨架和细胞點附而促进间质和血管内皮细胞形成毛细血管样结构;相反,抑制EphA2的活化可以削弱肿瘤的血管形成(Cheng et al. 2002)。因此,近年来EphA2/ephrin-Al在肿瘤中的作用越来越引起人们的关注,这一研究方向也为深入研究肿瘤细胞信号传导的作用机制开辟了一个新的领域。本文就此热点问题作一综述。
………
1 Eph家族及结构特征
Eph受体家族是1987年Hirai等(1987)在人类cDNA文库中蹄查病毒癌基因v加时发现的,被认为是具有独特特征的RTK家族。其他的RTK家族成员都是与可溶性的配体相结合而发挥作用,而Eph受体一般是与细胞膜表面偶联的ephrins配体相互作用而行使功能,这一特性与Eph受体和ephrins的结构特点是密不可分的。Eph受体与其ephrins配体均是单次跨膜蛋白。Eph受体胞外部分的末端为糖基化免疫球蛋白样的配体结合结构域,向下与一个富半耽氛酸区及两个型纤连蛋白重复区相连,通过跨膜序列达胞内,依次与胞膜卜结构域、酪氨酸激酶结构域、SAM(sterile alpha motif )及 PDZ ( Postsynaptic density 95-Discs large-Zonulaoccludentes-1 -protein)区相连,该受体蛋白中的蛋白激酶结构域与胞膜下结构域都含有略氨酸残基,酪氣酸残基憐酸化后可形成与含有SH2/SH3结构域信号分了的结合位点,介导经Eph受体的信号传导。Ephrin配体根据结构的同分为两大类,即ephrin-A和ephrin-B。Ephrin-A胞外结构域通过糖基磷脂酰肌醇(GPI)与细胞膜相偶联,没有跨膜及胞内结构;ephrin-B具有跨膜结构域及一段短的胞菜序列,即依次与保守的醋氨酸残基及PDZ结合位点链接,此胞内结构功能与Eph受体胞内结构类似,与含有SH2/SH3结构域的信号分子的结合有关(Cheng etal. 2002)。
……
第一部分eNOS/NO在ephrin-Al促HUYECs........ 19
第二部分PI3K/Akt信号通路在ephrin-Al/EphA2........ 35
第三部分低氧对口腔癌细胞膜偶联型........ 56
第三部分低氧对口腔癌细胞膜偶联型及分泌型ephr in-A1表达的影响
低氧是肿瘤微环境最重要的特征之一,可通过上调多种促血管生成因子的表达而调控肿瘤血管生成。Ephrin-Al以膜偶联型和分泌型两种形式存在,提示可能通过邻分泌和旁分泌的机制作用到邻近内皮细胞而促血管生成。本实验通过低氧干预SCC-9细胞,观察低氧刺激对两种类型ephrin-Al表达的影响,并运用细胞变圆实验验证可溶性ephrin-Al的生物学活性,试图建立肿瘤微环境中肿瘤细胞与内皮细胞的联系,进而阐明ephrin-Al促肿瘤血管生成的一种新机制。低氧是肿瘤微环境的重要特征之一,影响着肿瘤一系列生物学行为。我们用低氧培养箱培养SCC-9细胞,将低氧条件设置为37°C,1%02, 5%C02, 94%N2,以此模拟肿瘤低氧环境,观察低氧对SCC.9细胞GPI膜偶联型ephrin-Al及可溶性(分泌型)ephrin-Al表达的影响。
………..
结论
1. Ephrin-Al可通过增强HUVECs的迁移和成管能力而促血管生成;
2. eNOS/NO参与ephrin-A I的促血管生成过程,是ephrinA下游的关键效应分子;
3. P[3K/Akt信号通路介导了 ephrin-A l/EphA2与eNOS/NO之间的交互对话过程;
4.低氧剌激可上调SCC-9细胞膜偶联型和可溶性ephrin-A 1的表达;可溶性ephrin-A 1仍然保持了引发LJ-25I细胞形态改变的生物学活性。
…………
参考文献(略)
