本文是一篇医学论文,本研究首次阐明了MIF对人胚胎干细胞的具体作用及调控机制,对了解人胚胎干细胞的生理调控及其进一步的应用具有重要意义。
1.材料与方法
1.1实验材料
1.1.1选用细胞株
本实验使用人胚胎干细胞H9购自上海中乔新舟生物科技有限公司(ZQ0692)。293T细胞购自中科院细胞库(SCSP-502)。
1.1.2实验材料

1.2实验方法
1.2.1解冻复苏人胚胎干细胞实验
(1)培养器皿的基质包被:准备干净无菌的细胞培养板(本实验使用六孔板),抽取1mL Matrigel工作液包被细胞培养板。轻轻晃动培养板,将Matrigel工作液均匀地覆盖到培养孔的表面,使用前至少在37℃条件下孵育1h。
(2)将水浴槽内加入适量净水,预设水浴槽温度为37℃。
(3)将冻存的细胞从液氮储罐取出,迅速对冻存管标记信息进行核对,(将冻存管盖子松一下以防炸裂)将冻存管在水浴槽中快速晃动,使细胞快速融化,冻存管表面用75%乙醇擦拭,放置于超净台之内。
(4)融化后的细胞加入DMEM/F12培养基1mL,盖紧盖子并放入离心机中。
(5)配平,设置离心机300×g离心5min。
(6)移去上清液,将细胞沉淀轻轻用含有ROCK抑制剂Y27632的mTeSR1培养基2mL进行吹悬2-3次。
(7)轻轻地将培养板往一侧倾斜,使多余的Matrigel包被液在一侧的边缘汇聚,移去多余的Matrigel包被液,将细胞悬液移入培养板中,注意加入动作要轻柔,贴边注入,晃动培养板使细胞均匀平铺于器皿底部。
(8)在培养板上做好标记,放置在37℃,5% CO2细胞培养箱内。24h后,换新鲜的不加ROCK抑制剂Y27632的mTeSR1培养基。
2. 结果
2.1人胚胎干细胞的生长培养与自分泌
为了解人胚胎干细胞(H9)的生长状况,用CCK-8实验检测人胚胎干细胞的生长曲线(图2.1A),可以看到正常生长的细胞为大小相对均一、胞质较为透明的形态,似铺路石样,细胞排列紧密,呈集落状生长。H9的对数生长期在3-6天,后续实验均用此期细胞进行(图2.1B)。在细胞正常的生长情况下,取培养液进行ELISA实验,实验结果表明生理情况下分泌MIF约为20ng/mL(表2.1)。
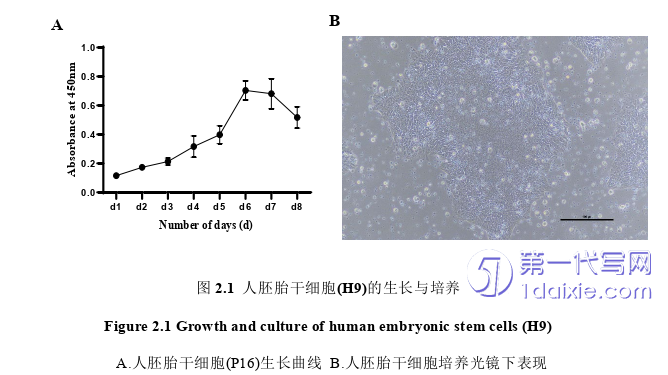
2.2 生理浓度的MIF促进人胚胎干细胞的增殖
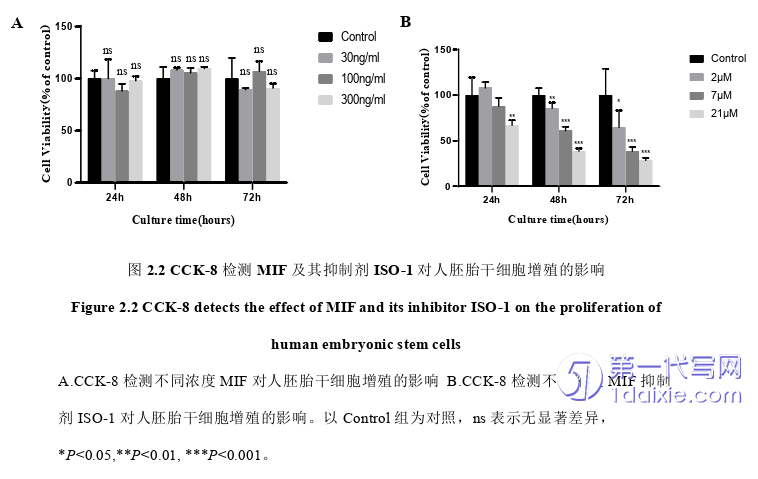
为明确MIF对于人胚胎干细胞的作用,外源性添加了不同浓度的MIF(30、100、300ng/mL)到人胚胎干细胞的培养基中培养,在24h、48h、72h用CCK-8检测结果显示,不同浓度的MIF对人胚胎干细胞的生长活力并无影响(图2.2A)。外源性添加不同浓度的MIF的抑制剂ISO-1(2、7、21μM)到人胚胎干细胞的培养基中培养,在24h、48h、72h用CCK-8检测结果显示,ISO-1能够抑制人胚胎干细胞的生长,且呈现剂量依赖性的趋势(图2.2B)。为彻底了解MIF对人胚胎干细胞的作用,本研究用CRISPR/Cas9双载体慢病毒质粒系统对人胚胎干细胞进行MIF基因的敲除,通过向人胚胎干细胞内导入Cas9和sgRNA序列表达框,进而实现对MIF基因的敲除。从图中可以看出,慢病毒成功感染不同组的细胞(图2.3A)。用qPCR检测,1-sgRNA成功地对细胞进行效率约为50%的敲除(图2.3B)。敲除MIF基因之后的人胚胎干细胞生长活力显著降低,最后甚至难以继续生长(图2.4)。
3. 讨论 ............................... 39
4. 结论 .............................. 44
3.讨论
MIF的表达和分泌谱表明,MIF在几乎所有哺乳动物细胞中都有表达,对许多生理过程至关重要[10]。MIF主要通过其受体以自分泌和旁分泌的方式参与细胞的增殖、迁移、凋亡、分化等生物学功能。先前已经有过人胚胎干细胞自分泌MIF的相关研究,然而MIF对人胚胎干细胞的具体作用及其调控机制还尚未可知。因此,本研究首次阐明了MIF对人胚胎干细胞的具体作用及调控机制,对了解人胚胎干细胞的生理调控及其进一步的应用具有重要意义。
已有研究证明MIF能促进多种细胞的增殖存活。研究证明MIF通过AKT、ERK、AMPK、Wnt/β-catenin等多种通路促进神经干细胞的存活、增殖[18, 19]。MIF通过调节AKT-FOXO3a信号通路中的氧化应激,保护间充质干细胞免受缺氧/饥饿诱导的细胞凋亡[22]。鉴于MIF在细胞增殖和存活中的这些作用,研究还发现多种肿瘤高表达MIF,包括多形性胶质母细胞瘤、黑色素瘤、前列腺癌、胃癌、胰腺癌和肺癌[32-34]。越来越多的研究表明,血清中MIF的异常浓度反映了患者的病理状态。健康对照组的血清MIF浓度在0.2-8.3ng/mL之间[10]。而在不同的病理情况下,血清平均MIF浓度不同:登革热休克综合征(102ng/mL)、食管鳞状细胞癌(100ng/mL)、肺结核(19.84ng/mL),多发性肌炎(50ng/mL),白癜风(32.96ng/mL),牙周炎(71.8ng/mL)和严重败血症(103.7ng/mL)[10]。研究结果显示,正常生长的人胚胎干细胞能够自分泌大约20ng/mL的MIF。为了探究人胚胎干细胞分泌如此高浓度的MIF的作用,本研究外源性添加不同浓度的MIF对人胚胎干细胞的增殖无影响,而通过添加MIF抑制剂ISO-1或者敲除细胞中的MIF,人胚胎干细胞的增殖和存活受到严重抑制,敲除MIF后的细胞甚至无法存活。MIF与其他因子的不同之处在于,MIF是半组成型表达,并且是预先从储存池中分泌到体内循环,以维持细胞的正常生理功能[35]。以上研究充分说明在正常的机体中能够恒定表达MIF,其生理浓度的MIF对于机体的正常生存必不可少
4.结论
1.人胚胎干细胞自分泌MIF,其自分泌的生理浓度约为20ng/mL,生理浓度的MIF促进人胚胎干细胞的增殖,并且对人胚胎干细胞的存活至关重要。
2.高于生理浓度的MIF通过降低KLF4的表达抑制人胚胎干细胞的自我更新,通过促进FOXA2的表达开启人胚胎干细胞分化的第一步。
3.MIF可能通过β-arrestin1介导的CXCR4内化来调控对人胚胎干细胞的信号传递。
参考文献(略)
